Index⚓
Glossaire⚓
A-B
- Adiabatique
Une transformation adiabatique (ou processus adiabatique) est une transformation qui ne produit pas d'échange de chaleur avec le milieu extérieur \(\left (Q = 0\right )\).
Ce type de transformation a lieu lorsque le système thermodynamique (dans ce cas un gaz parfait) se trouve dans un récipient isolé de l'extérieur par l'intermédiaire de parois adiabatiques. Les transformations qui se produisent très rapidement et pour lesquelles le système n'a pas le temps d'échanger de la chaleur avec le milieu extérieur peuvent elles aussi être considérées comme étant adiabatiques.
- Adiabatique
Une transformation adiabatique (ou processus adiabatique) est une transformation qui ne produit pas d'échange de chaleur avec le milieu extérieur \(\left (Q = 0\right )\).
Ce type de transformation a lieu lorsque le système thermodynamique (dans ce cas un gaz parfait) se trouve dans un récipient isolé de l'extérieur par l'intermédiaire de parois adiabatiques. Les transformations qui se produisent très rapidement et pour lesquelles le système n'a pas le temps d'échanger de la chaleur avec le milieu extérieur peuvent elles aussi être considérées comme étant adiabatiques.
- Atomes ou molécules ?
Vous avez peut-être du mal à retenir ce qu'est un atome ou une molécule. Voici une petite analogie qui devrait permettre de ne plus confondre.
Un atome c'est une lettre.
Une molécule c'est un mot.
Un mot est composé de lettres qui sont liées entre elles (du moins dans l'écriture courante); une molécule est composée d'atomes liés entre eux.
L'alphabet est composé de 26 lettres ; l'alphabet de la matière est composé, lui, d'environ cent atomes.
Avec 26 lettres on peut écrire un grand nombre de mots mais tous les mots n'existent pas ; avec cent atomes les combinaisons d'atomes pour former des molécules sont très grandes mais toutes n'existent pas.
Un mot c'est une suite ordonnée de lettres; dans une molécule les atomes ne sont pas liés entre eux de n'importe quelle façon.
C-D
- Capacité thermique
La capacité thermique d'un objet tient déjà compte de la masse de l'objet contrairement à la capacité thermique massique d'un corps.
La capacité thermique d'un objet est donc définie pour l'objet dans son entièreté . Quelque ce soit la masse de cet objet, sa capacité thermique tiendra donc déjà compte de sa masse.
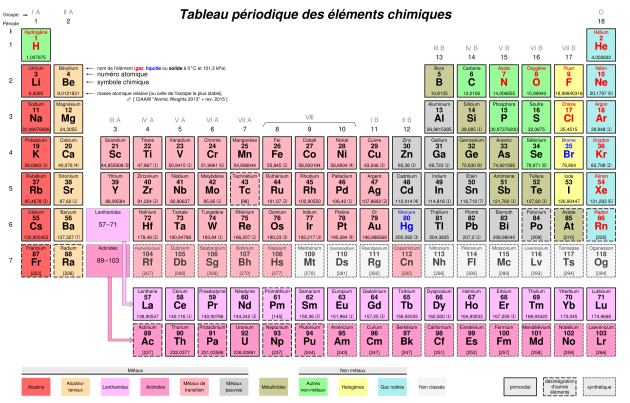
- Classification périodique
Tableau périodique des éléments | Informations[*] - Coefficient stœchiométrique
Le coefficient (ou nombre) stœchiométrique d'une espèce chimique dans une réaction chimique donnée est le nombre qui précède sa formule dans l'équation considérée (un, à défaut). Dans l'exemple suivant :
\(\ce{CH4 + 2\ O2 -> CO2 + 2\ H2O}\)
le nombre stœchiométrique du méthane \(\ce{CH4}\) est 1, celui du dioxygène \(\ce{O2}\) est 2, celui du dioxyde de carbone est 1 et celui de l'eau \(\ce{H2O}\) est 2.
- Concentration en masse
La concentration en masse \(\gamma\) (lettre grecque gamma) \(\mathrm{ \left (en \; g.L^{-1} \right)}\) d'un soluté est la masse \(\mathrm{ m\; \left ( en\; g \right ) }\) de soluté dissous dans le volume \(\mathrm{ V\; \left ( en\; L \right ) }\) de la solution.
\(\mathrm{ \gamma = \dfrac{m}{V}}\).
Exemple : si on dissout \(1\; g\) de sel dans \(1/2\; L\) de soupe, la concentration en sel de la soupe sera de : \(\mathrm{ \gamma_{sel} = \dfrac{1}{0,5} = 2 \; g/L}\).
- Couche externe
C'est la dernière couche qui contient au moins un électron. Elle peut être composée de plusieurs sous-couches.
- Détergents
Un détergent (ou agent de surface, détersif, surfactant) est un composé chimique, généralement issu du pétrole, doté de propriétés tensioactives, ce qui le rend capable d'enlever les salissures.
La détersion est un élément d'hygiène fondamental, puisqu'il permet d'éliminer une grande partie des bactéries présentes en particulier sur la peau, et sur les ustensiles servant à la préparation et à la consommation des repas.
(Source : https://fr.wikipedia.org/wiki/D%C3%A9tergent )
- Ductilité
En résistance des matériaux, la ductilité désigne la capacité d'un matériau à se déformer plastiquement sans se rompre.
La rupture se fait lorsqu'un défaut (fissure ou cavité), induit par la déformation plastique, devient critique et se propage. La ductilité est donc l'aptitude d'un matériau à résister à cette propagation. S'il y résiste bien, il est dit ductile, sinon il est dit fragile.
E
- Électron de valence
C'est un électron présent dans la couche externe de la structure électronique.
(Ces électrons sont ceux qui permettent de créer des liaisons chimiques).
- Élément chimique
C'est un noyau caractérisé par son numéro atomique.
- Émulsifiant - Émulsion
Substance qui favorise la formation et/ou la stabilisation d'une émulsion.
Émulsion :
Une émulsion est un mélange hétérogène de deux substances liquides non miscibles, l'une étant dispersée sous forme de petites gouttelettes dans l'autre. Ce sont toujours deux liquides qui ne se mélangent pas spontanément (non miscibles), comme l'eau et l'huile, mais qui vont grâce à des opérations spécifiques (agitation, mélange, ajout de quelques principes actifs) adopter un aspect macroscopiquement homogène, mais microscopiquement hétérogène. L'une des substances sera donc dispersée dans la seconde substance sous forme de gouttelettes. Le mélange reste stable grâce à un troisième ingrédient appelé émulsifiant (vitesse ou cinétique d'évolution du mélange quasi nulle).
Une mousse ressemble à une émulsion mais la seconde substance est un gaz (au lieu d'un liquide), dispersé sous forme de bulles. Une autre différence importante entre mousses et émulsions est la fraction volumique de la phase dispersée (gaz), en général beaucoup plus élevée dans les mousses les plus stables.
- enceinte isolée
Une enceinte isolée est une enceinte qui ne permet pas l'échange de matière ni d'énergie avec le milieu extérieur.
- énergie cinétique
Il s'agit de l'énergie liée au mouvement des objets ou des particules.
F-L
- Famille chimique
C'est une colonne de la classification périodique.
- Fusion
C'est le nom du changement d'état de l'état solide à l'état liquide. Rappel : lors d'un changement d'état la température reste constante.
Il s'agit d'une transformation physique.
- Grandeur physique
Une grandeur physique est un ensemble d'unités de mesure, de variables, d'ordres de grandeur et de méthodes de mesure (qui sont l'objet de la métrologie) lié à un aspect ou phénomène particulier de la physique. Par exemple, la grandeur longueur regroupe tout ce qui concerne les distances.
----
L'addition et la soustraction sont seulement possible entre données de même grandeur. En revanche, il est possible de multiplier ou de diviser des grandeurs différentes, auquel cas on obtient une nouvelle grandeur dérivée des deux autres.
----
Par exemple, la vitesse est issue de la division de la longueur par le temps. Il existe donc théoriquement une infinité de grandeurs, mais seul un certain nombre d'entre elles sont utilisées dans la pratique. Le domaine de la physique qui traite des relations entre les grandeurs est l'analyse dimensionnelle.
__
Source et plus d'informations : https://www.techno-science.net/definition/1695.html
- Isoélectronique
Deux espèces chimiques sont isoélectroniques si elles possèdent le même nombre d'électrons, et donc la même structure électronique.
- Liquide mouillant
Le mouillage est le comportement d'un liquide en contact avec une surface solide.
Il désigne d'une part la forme que prend le liquide à la surface du solide (mouillage statique) et la façon dont il se comporte lorsqu'on essaie de le faire couler (ancrage, mouillage dynamique).
Ces comportements découlent des interactions intermoléculaires entre les molécules de liquide, solide et de gaz à l'interface entre les trois milieux. Ces interactions sont modélisées à l'échelle macroscopique via la tension superficielle.
(Source : https://fr.wikipedia.org/wiki/Mouillage_(physique) )
M
- Malléabilité
La malléabilité est la raison pour laquelle on peut laminer (rouleau compresseur) un matériau, le forger (martèlement), ou découper facilement une faible épaisseur.
L'or, l'argent et le plomb sont des métaux très malléables ou ductiles.
- Masse volumique
La masse volumique d'une substance, aussi appelée densité volumique de masse, est une grandeur physique[*] qui caractérise la masse de cette substance par unité de volume.
Cette grandeur physique est généralement notée par les lettres grecques \(\rho\) (rhô) ou \(\mu\) (mu). On utilise ces deux notations en fonction des habitudes du domaine de travail. Toutefois, le Bureau international des poids et mesures (BIPM) recommande d'utiliser la notation \(\rho\).
Plus d'infos : https://fr.wikipedia.org/wiki/Masse_volumique
- microscopique
Très petit, minuscule, qui ne peut être aperçu qu'à l'aide d'un microscope.
- Moussant
Qui produit de la mousse : Savon moussant.
Réactif utilisé dans la flottation pour permettre de donner une écume stable en abaissant la tension superficielle de l'eau. (L'huile de pin est un moussant classique.)
Pouvoir moussant : degré d'aptitude des solutions de surfactifs à donner naissance à des mousses, en présence d'air ou d'autres gaz au sein du liquide.
N-P
- Ordre de grandeur
Un ordre de grandeur est un nombre qui représente de façon simplifiée mais approximative la mesure d'une grandeur physique[*]. Ce nombre, le plus souvent une puissance de 10, est utilisé notamment pour communiquer sur des valeurs très grandes ou très petites, comme le diamètre du système solaire ou la charge d'un électron.
L'ordre de grandeur se mémorise plus facilement qu'une valeur précise et suffit pour de nombreux usages. Il est également utile dans les domaines intermédiaires pour situer la taille d'un objet ou pour choisir la gamme d'appareils de mesure à lui appliquer.
L'ordre de grandeur d'une valeur est sa plus proche puissance de 10.
Plus d'info : https://fr.wikipedia.org/wiki/Ordre_de_grandeur
- Période
C'est le nom donné à une ligne du tableau périodique.
- Proportions stoéchiométriques
Pour une réaction chimique modélisée par l'équation : \(\ce{\mathbf{a}\ A + \mathbf{b}\ B -> \mathbf{c}\ C + \mathbf{d}\ D}\), les nombres \(\mathbf{a}\), \(\mathbf{b}\), \(\mathbf{c}\) et \(\mathbf{d}\) sont les coefficients stœchiométriques des espèces chimiques A, B, C et D.
Les réactifs sont introduits dans les proportions stœchiométriques si \(\dfrac{\left(n_{A}\right)_i}{\mathbf{a}}=\dfrac{\left(n_{B}\right)_i}{\mathbf{b}}\).
Pour les produits, on aura : \(\dfrac{\left(n_{C}\right)_f}{\mathbf{c}}=\dfrac{\left(n_{D}\right)_f}{\mathbf{d}}\).
Q-Z
- Structure électronique réorganisée par n° de couche
Une structure électronique réorganisée par n° de couche au lieu de l'ordre de la règle de Klechkowski devra s'écrire ainsi :
\(\mathrm{1s\; \;\;2s \:2p\;\;\;3s\:3p\:3d\;\;\;4s \:4p \:4d\:4f\;\;\;5s\;...}\)
- système
Le système est l'ensemble des éléments étudiés qui vont participer aux échanges d'énergie de l'étude. Tous les autres éléments seront considérés comme extérieur au système, donc non étudiés.
Il est très important de bien définir le système étudié au début de chaque étude.
- Valeur en eau
La valeur en eau d'un objet est la masse d'eau équivalente à cet objet pour les transferts thermiques.
Par exemple, la valeur en eau d'un calorimètre et de ses accessoires correspond à la masse d'eau équivalente permettant de réaliser les même transferts thermiques.