📄 Documents et définitions 📌⚓
Complément : 📚 Document n°1 : La mole (📌 Définition à savoir📌)
Une mole[*] est un paquet de \(6,022\cdot 10^{23} \ \mathrm{mol^{-1}}\) entités. Ce nombre est fixe, quelle que soit l’entité considérée. Il s’agit du même fonctionnement qu’un pack de bouteilles ; en effet, un pack de 6 contient toujours 6 bouteilles, quelle que soit la nature de la bouteille.


Un pack de bouteilles d’eau contient 6 bouteilles d’eau.
Une mole de soufre contient \(\mathbf{6,022\cdot 10^{23} \ \mathrm{mol^{-1}}}\) atomes de soufre
_____________________________________________________________________________________________________


Un pack de bouteilles d’Orangina contient 6 bouteilles d’Orangina
Une mole de glace contient \(\mathbf{ 6,022\cdot 10^{23} \ \mathrm{mol^{-1}}}\) molécule d'eau
Complément : 📚 Document n°2 : La masse molaire (📌 Définition à savoir📌)
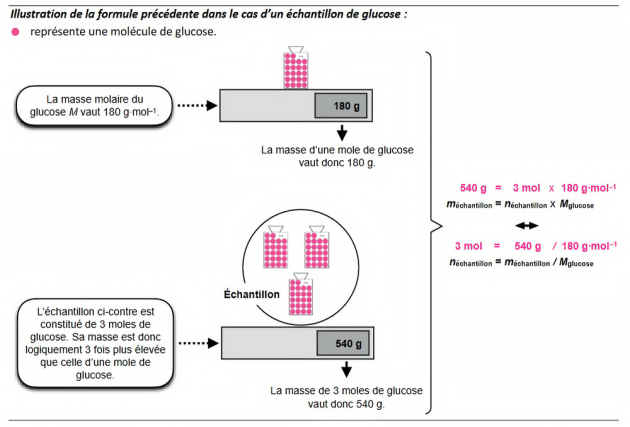
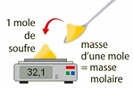
La masse molaire d’une espèce chimique, en \(\mathrm{g/mol}\), est la masse d’une mole de cette espèce.
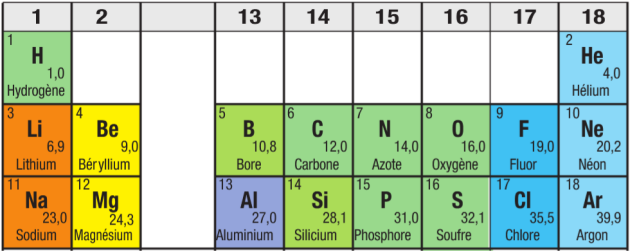
Si l’espèce est composée d’un seul élément, alors sa masse molaire est indiquée dans le tableau périodique. On dit que c’est la masse molaire de l’atome qui correspond à l’élément.
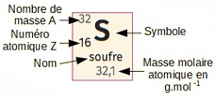
Si l’espèce est composée de plusieurs éléments, alors sa masse molaire se calcule en additionnant les masses molaires des éléments en fonction de leur répartition.
On dit également que c’est la masse molaire de l’entité qui la compose. Par exemple, la masse molaire d’une espèce moléculaire est la somme des masses molaires des atomes qui composent la molécule.
\(M \left( \ce{C6H12} \right)=6\times M\left( \ce{C} \right)+12\times M\left( \ce{H} \right)=6 \times 12,0 + 12 \times 1,0=84,0\ \mathrm{g \cdot mol^{-1}}\)
Pour un échantillon de masse en , la quantité de matière , ou nombre de moles, vaut : \[\definecolor{grisRGB}{RGB}{225, 225, 225} {\fcolorbox{red}{grisRGB}{$ \begin{array}{rcl} \mathbf{\Large n = \dfrac{m}{M} } \end{array} $}}\]

Complément : 📚 Document n°3 : Trois espèces chimiques
Solide | Sel de table | Sucre | Bicarbonate de sodium |
Formule | \(\ce{NaC\ell}\) | \(\ce{C6H12O6}\) | \(\ce{NaHCO3}\) |
❓Questions⚓
Question⚓
Q1. Calculer la masse molaire des trois espèces chimiques du Document 3.
Solution⚓
Q1.
\(M_\mathrm{\ce{NaC\ell}}=M_\mathrm{\ce{Na}}+M_\mathrm{\ce{C\ell}}=23,0+35,5=58,5\ \mathrm{g\cdot mol^{-1}}\)
\(M_\mathrm{\ce{C6H12O6}}=6\times M_\mathrm{\ce{C}}+12\times M_\mathrm{\ce{H}} + 6\times M_\mathrm{\ce{O}}=6 \times 12,0 + 12 \times 1,00+6 \times 16,0=180,0\ \mathrm{g\cdot mol^{-1}}\)
\(M_\mathrm{\ce{NaHCO3}}= M_\mathrm{\ce{Na}}+ M_\mathrm{\ce{H}} + M_\mathrm{\ce{C}} + 3\times M_\mathrm{\ce{O}}=23,0 + 1,00 + 12,0 + 3 \times 16,0=84,0\ \mathrm{g\cdot mol^{-1}}\)
Question⚓
Q2. Pour chaque solide, calculer la masse qui correspond à une quantité de matière \(n=0,010\ \mathrm{mol}\).
Solution⚓
Q2.
\(n=\dfrac{m}{M} \iff m=n \times M\)
\(m_\mathrm{\ce{NaC\ell}}=n \times M_\mathrm{\ce{NaC\ell}}=0,010 \times 58,5=5,85\cdot 10^{-1}\ \mathrm{g}\)
\(m_\mathrm{\ce{C6H12O6}}=n \times M_\mathrm{\ce{C6H12O6}}=0,010 \times 180,0=1,80\ \mathrm{g}\)
\(m_\mathrm{\ce{NaHCO3}}=n \times M_\mathrm{\ce{NaHCO3}}=0,010 \times 84,0=8,40\cdot 10^{-1}\ \mathrm{g}\)
Question⚓
Q3. Pour chaque solide, calculer la quantité de matière contenue dans \(m=20,0\ \mathrm{g}\).
Solution⚓
Q3.
\(n_\mathrm{\ce{NaC\ell}}=\dfrac{m}{M_\mathrm{\ce{NaC\ell}}}=\dfrac{20,0}{58,5} =3,42\cdot 10^{-1}\ \mathrm{mol}\)
\(n_\mathrm{\ce{C6H12O6}}=\dfrac{m}{M_\mathrm{\ce{C6H12O6}}}=\dfrac{20,0}{180,0}=0,111\ \mathrm{mol}\)
\(n_\mathrm{\ce{NaHCO3}}=\dfrac{m}{M_\mathrm{\ce{NaHCO3}}}=\dfrac{20,0}{84,0} =2,38\cdot 10^{-1}\ \mathrm{mol}\)
Complément : 📚 Document n°5 : La concentration en quantité de matière
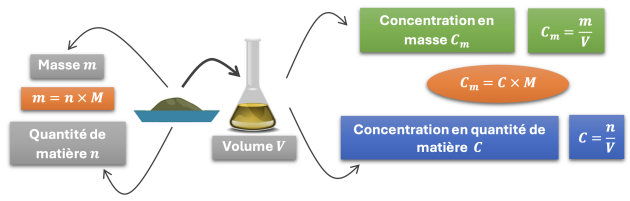
La concentration en masse d’une solution notée \(C_m\), correspond à la masse de soluté dissoute dans un litre de solution. Elle s’exprime en \(\mathbf{g/L}\).
Cette masse de soluté contient une quantité de matière de soluté. On peut alors définir la concentration en quantité de matière de cette solution comme la quantité de matière de soluté contenue dans un litre de solution. Elle s’exprime en \(\mathbf{mol/L}\).
Question⚓
Q4. On dissout \(m=4,0\ \mathrm{g}\) de sel dans de l’eau pour obtenir \(V=500 \ \mathrm{mL}\) de solution. Calculer la concentration en masse \(C_m\) de la solution préparée en veillant à respecter le nombre de chiffres significatifs.
Question⚓
Q5. Déterminer la concentration en quantité de matière.