🎯 Objectif
① Exploiter la relation entre le pH d’une solution et la concentration en ions \(\ce{H3O+}\)
Complément : 📜 Introduction
La pollution atmosphérique et l’humidité contribuent chaque jour à l’encrassement des façades et à la formation de salissures vertes et noires sur les parois des bâtiments, qui sont souvent solidement incrustées dans les matériaux et ne sont pas faciles à nettoyer. Pour cela, il existe deux types de produits :
Les nettoyants façade acide : les traitements au pH 0, pH 1 et pH 2 sont des nettoyants pour façade plus ou moins acides. L’action de nettoyage se fait par réaction chimique dans laquelle le produit acide attaque la salissure sur le support avec une grande efficacité. Ce type de nettoyant convient à de nombreux matériaux dans le bâtiment : béton, briques, marbre, grès…
Les nettoyants façade alcalins : les traitements au pH 11 et pH 14 sont des produits nettoyants pour façade alcalins. Avec ce type de produits, le principe actif transforme les graisses en savon afin de pouvoir les éliminer au rinçage. Les nettoyants pour façade alcalins conviennent particulièrement au nettoyage des supports en pierres calcaires.
Source : https://www.eurochem-france.fr/22-produit-nettoyage-facade
🔍 Problématique : Que mesure et comment mesurer le pH ?⚓
On dispose d’une solution d’acide chlorydrique de concentration \(C_0=1{,}0\times 10^{-2}\ \mathrm{mol\cdot L^{-1}}\).
Il s’agit d’un acide fort (notion qui sera abordée dans une autre activité). La concentration en acide fort est donc égale à la concentration en ion oxonium, notée \(\Big[ \ce{H3O+} \Big]\).
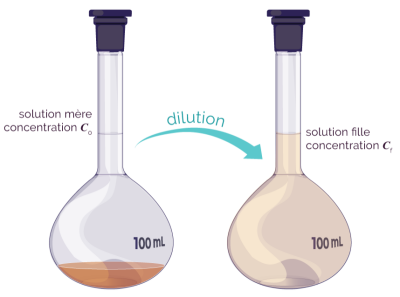
Complément : 📄 Document n°1 : La dilution 💧
La dilution consiste à prélever un volume de la solution mère et à lui ajouter de l'eau distillée pour obtenir la solution fille.
On appelle facteur de dilution, noté \(F\), le rapport entre la concentration de la solution mère, \(C_0\), et la concentration de la solution fille, \(C_f\).
\[\hspace{4cm} {\fcolorbox{red}{white}{$ { \ \ \ \mathbf{ F = \dfrac{\hspace{2mm} C_0 \hspace{2mm} }{ C_f } } \ \ \ } $}}\]
Le volume de solution mère, \(V_0\), à prélever pour préparer une solution fille de volume \(V_f\) est donc :
\[\hspace{4cm} \ \ \ \mathbf{ V_0 = \dfrac{\hspace{2mm} V_f \hspace{2mm} }{ F } } \]
On souhaite préparer 3 solutions filles d’un volume \(V_f=100 mL\) à partir de la solution d’acide chlorhydrique.
Voici un tableau qu'il faudra compléter en répondant aux questions ci-dessous.
Solution | 0 | 1 | 2 | 3 |
|---|---|---|---|---|
Facteur de Dilution | X | \(10\) | \(20\) | \(100\) |
Volume en mL à prélever. | X |
|
|
|
Concentration en ions oxonium \(\left[ \ce{H3O+} \right]\) en \(\mathrm{mol\cdot L^{-1}}\) |
|
|
|
|
pH mesuré (méthode 1) |
|
|
|
|
pH mesuré (méthode 2) |
|
|
|
|
pH calculé |
|
|
|
|
1️⃣ 1ère partie : Préparation des solutions, et mesure de pH (méthode 1)⚓
Question⚓
Q1. Déterminer le volume de solution mère à prélever pour chacune des solutions et compléter la 3ème ligne du tableau.
Solution⚓
Q1.
On utilise la deuxième formule du document n°1 :\[\hspace{4cm} \ \ \ \mathbf{ V_0 = \dfrac{\hspace{2mm} V_f \hspace{2mm} }{ F } } \]
Solution | 0 | 1 | 2 | 3 |
|---|---|---|---|---|
Facteur de Dilution | X | \(10\) | \(20\) | \(100\) |
Volume en mL à prélever. | X | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB}10{,}0\ \mathrm{mL}\) | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB}5{,}0\ \mathrm{mL}\) | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB} 1{,}0\ \mathrm{mL}\) |
Question⚓
Q2. Calculer la concentration des 3 solutions, et compléter le 4ème ligne du tableau.
Solution⚓
Q2.
Il faut employer la première formule du document n°1 : \(C_f=\dfrac{C_0}{F}\) sachant que \(C_0=1{,}0\times 10^{-2}\ \mathrm{mol\cdot L^{-1}}\)
Solution | 0 | 1 | 2 | 3 |
|---|---|---|---|---|
Facteur de Dilution | X | \(10\) | \(20\) | \(100\) |
Concentration en ions oxonium \(\left[ \ce{H3O+} \right]\) en \(\mathrm{mol\cdot L^{-1}}\) | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB}1{,}0\times 10^{-2}\) | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB}1{,}0\times 10^{-3}\) | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB}5{,}0\times 10^{-4}\) | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB}1{,}0\times 10^{-4}\) |
📝 Protocole expérimental - À compléter ✍️
Question⚓
Q4. Réaliser, après validation du protocole, les 3 solutions, puis faire un schéma des étapes clés de la dilution (pour une seule solution).
2️⃣ Partie n°2 : Mesure précise du pH⚓
Complément : 📄 Document n°2 : Le pH-mètre 📟
Un pH-mètre[*] est un appareil permettant la mesure du pH d'une solution. Il est constitué d'un boîtier électronique permettant l'affichage de la valeur numérique du pH et d'une sonde de pH constituée d'une électrode de verre permettant la mesure et d'une électrode de référence.
L’électrode de verre est très fragile, et il ne faut pas la laisser à l’air libre.
Avant utilisation, l'appareil doit être étalonné au moyen de deux solutions tampon (pH 4, 7 et 10 disponibles).
Entre chaque utiliser, il faut rincer les électrodes à l’eau distillée et la sécher délicatement.
Question⚓
Q9. Comparer les deux méthodes de mesures en présentant les avantages et les inconvénients.
Solution⚓
Q9.
Le papier pH[*] permet de mesurer le pH rapidement et facilement, mais la valeur obtenue est approximative car elle dépend de la comparaison des couleurs.
Le pH‑mètre[*], quant à lui, donne une mesure précise et fiable du pH, mais il est plus coûteux et nécessite un étalonnage.
Ainsi, le papier pH est utilisé pour une estimation rapide, tandis que le pH‑mètre est utilisé lorsque l’on a besoin de précision.
🤔 Qu'est-ce que le pH ? 🧪⚓
Définition : 📄 Document n°3 : Définition du pH (📍 À Savoir 📌)
Le potentiel hydrogène, noté pH, permet de mesurer l’acidité ou la basicité d’une solution. Il est lié à la concentration en ions oxonium \(\ce{H3O+}\) dans la solution.
La valeur du pH est un nombre sans unité compris entre 0 et 14.
Le pH des solutions diluées (concentration inférieur à \(0{,}10\ \mathrm{mol\cdot L^{-1}}\)) est défini par l'expression simplifiée :
\[\hspace{7cm}{\fcolorbox{red}{white}{$ { \ \ \ \mathbf{ pH = -\log \Big[ \ce{H3O+} \Big] } \ \ \ } $}}\]
Et réciproquement :
\[\hspace{7.3cm}{\fcolorbox{red}{white}{$ { \ \ \ \mathbf{ \Big[ \ce{H3O+} \Big] = 10^{pH } } \ \ \ } $}}\]
Question⚓
Q11. Calculer le pH des solutions et compléter la dernière ligne du tableau.
Solution⚓
Q11.
Solution | 0 | 1 | 2 | 3 |
|---|---|---|---|---|
Facteur de Dilution | X | \(10\) | \(20\) | \(100\) |
Volume en mL à prélever. | X | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB}10{,}0\ \mathrm{mL}\) | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB}5{,}0\ \mathrm{mL}\) | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB} 1{,}0\ \mathrm{mL}\) |
Concentration en ions oxonium \(\left[ \ce{H3O+} \right]\) en \(\mathrm{mol\cdot L^{-1}}\) | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB}1{,}0\times 10^{-2}\) | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB}1{,}0\times 10^{-3}\) | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB}5{,}0\times 10^{-4}\) | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB}1{,}0\times 10^{-4}\) |
pH mesuré (méthode 1) | \(......\) | \(......\) | \(......\) | \(......\) |
pH mesuré (méthode 2) | \(......\) | \(......\) | \(......\) | \(......\) |
pH calculé | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB}2{,}0\) | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB}4{,}0\) | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB}3{,}3\) | \(\definecolor{violetRGB}{RGB}{145, 0, 255}\color{violetRGB}4{,}0\) |
On peut déterminer que le pH-mètre a une incertitude-type de \(\pm 0,05\). Cela signifie que la valeur de pH mesuré est juste, si la valeur théorique de pH est comprise entre les valeurs \(\left( pH_\text{mesuré}-0,05 \right)\) et \(\left( pH_\text{mesuré}+0,05 \right)\).
Question⚓
Q12. Indiquer si les valeurs mesurées sont justes. Sinon identifier une source d’erreur.
Solution⚓
Q12.
Les valeurs de pH obtenues expérimentalement (papier pH et pH‑mètre) sont cohérentes entre elles et avec la valeur théorique, bien qu’elles ne soient pas strictement identiques. Elles peuvent donc être considérées comme acceptables dans le cadre de l’activité, compte tenu des incertitudes expérimentales.
Les écarts observés s’expliquent par plusieurs sources d’erreur :
Mesure au papier pH :
méthode intrinsèquement peu précise (lecture à l’unité de pH près) ;
subjectivité de la lecture colorimétrique ;
influence possible de l’éclairage ou de la coloration de la solution.
Mesure au pH‑mètre :
incertitude liée à un étalonnage imparfait ;
état de l’électrode (rinçage, immersion, vieillissement) ;
influence éventuelle de la température de la solution.
Valeur calculée :
valeur théorique établie dans des conditions idéales (solution parfaitement homogène, concentration exacte), rarement totalement atteintes expérimentalement.
Conclusion pédagogique :
Les différences entre pH mesuré et pH calculé sont normales et illustrent les limites des méthodes de mesure ainsi que la distinction entre modèle théorique et réalité expérimentale. L’activité permet ainsi de travailler la notion d’incertitude de mesure et de validité des résultats expérimentaux.
Question⚓
Q13. Conclure en répondant à la problématique.
Solution⚓
Q13.
Le pH est une grandeur qui permet de caractériser l’acidité ou la basicité d’une solution aqueuse. Il est lié à la concentration en ions oxonium \(\ce{H3O+}\) : plus cette concentration est élevée, plus le pH est faible et la solution est acide.
Le pH peut être mesuré :
de manière approchée à l’aide du papier pH, par comparaison de couleurs ;
de manière précise à l’aide d’un pH‑mètre, qui fournit une valeur numérique fiable.
Ainsi, le choix de la méthode de mesure dépend du niveau de précision recherché. La comparaison entre pH mesuré et pH calculé met en évidence les limites expérimentales et souligne l’écart possible entre modèle théorique et réalité expérimentale.