📌 Définitions de la solubilité 📍⚓
Définition : (📌 À Savoir 📍)
La solubilité molaire \(\mathbf{s}\) d'une espèce dans un solvant est égale à la quantité de matière maximale de solide que l'on peut dissoudre dans un litre de solution. Elle s'exprime en \(\mathrm{mol \cdot L^{-1}}\).
La solubilité massique \(\mathbf{s_m}\) d'une espèce dans un solvant est égale à la masse maximale de solide que l'on peut dissoudre dans un litre de solution. Elle s'exprime en \(\mathrm{g \cdot L^{-1}}\).
Les solubilités molaire et massique sont liées par la relation : \[\definecolor{grisRGB}{RGB}{225, 225, 225} {\fcolorbox{red}{grisRGB}{$ \begin{array}{rcl} \mathbf{\Large s = \dfrac{s_m}{M} } \end{array} $}}\]
Lorsqu'un solide est dissous dans un solvant, une solution homogène est obtenue. Si la concentration atteint la valeur de la solubilité, on dit que la solution est saturée.
Une solution est dite saturée lorsqu'il n'est plus possible, à une température donnée, d'augmenter la quantité de matière de soluté dissous dans le solvant. Au-delà de la limite de saturation, il reste du solide non dissous : le mélange est hétérogène.
Exemple : 📚
La solubilité massique du chlorure de sodium \(\ce{NaC\ell}\) dans l'eau, à \(20\ \mathrm{^\circ C}\), est \(s_\mathrm{m, \ce{NaC\ell}} = 358,5\ \mathrm{g \cdot L^{-1}}\). Si nous introduisons, dans \(1\ \mathrm{L}\) d'eau, une masse de chlorure de sodium maci égale à \(400\ \mathrm{g}\), la solution obtenue sera saturée et sa concentration en masse égale à \(358,5 \ \mathrm{g \cdot L^{-1}}\). Il restera alors une masse égale à \(400 - 358,5 = 41,5\ \mathrm{g}\) de chlorure de sodium non dissous. Nous obtenons donc un mélange hétérogène.
💪🏻 Exercice d'application⚓
Données :
Masse molaire du glucose : \(M_\textsf{glucose} = 180\ \mathrm{g \cdot mol^{-1}}\) ;
Solubilité molaire du glucose à \(20\ \mathrm{^\circ C}\) : \(s_\textsf{glucose} = 3,89 \ \mathrm{mol \cdot L^{-1}}\)
Question⚓
Q1. Indiquer si une solution aqueuse de glucose à la concentration \(C_\textsf{m, glucose} = 500\ \mathrm{g \cdot L^{-1}}\) est saturée.
Solution⚓
Q1.
On donne la solubilité molaire, et on a la concentration en masse. Convertissons la concentration en concentration en quantité de matière :
\(C_\textsf{glucose} =\dfrac{C_\textsf{m, glucose} }{M_\textsf{m, glucose} }=\dfrac{500}{180}=2,8\ \mathrm{mol \cdot L^{-1}}\)
On a donc \(C_\textsf{glucose}<s_\textsf{glucose}\) donc la solution n'est pas saturée.
Question⚓
Q2. Calculer la masse maximale de glucose \(m_\textsf{max}\) que l'on peut dissoudre dans un volume \(V = 100\ \mathrm{mL}\) de solution.
Solution⚓
Q2.
La masse maximale que l'on peut dissoudre dans \(V = 100\ \mathrm{mL}\) de solution est :
\(m_\textsf{max, glucose}={\color{blue} n_\textsf{max, glucose}} \times M_\textsf{glucose}={\color{blue}s_\textsf{glucose} \times V_\textsf{sol} } \times M_\textsf{glucose}\)
\(m_\textsf{max, glucose}={\color{blue}3,89\times100\cdot 10^{-3}} \times 180\)
\(\definecolor{rougeFonceRGB}{RGB}{192, 0, 0}\color{rougeFonceRGB}m_\textsf{max, glucose}=70\ \mathrm{g}\)
📈 Évolution de la solubilité (📝 Travail à faire sur une feuille 📝)⚓
🎯 Objectif
Mettre en œuvre un protocole pour étudier l'influence du pH et de la température sur la solubilité d'une espèce chimique.
Complément : Document n°1 : L'acide benzoïque
L'acide benzoïque, dont la structure est représentée ci-contre, est un solide utilisé notamment comme conservateur dans l'industrie alimentaire. Il est référencé en Europe sous l e code E210. L'acide benzoïque est peu soluble dans l'eau et en milieu acide en raison de la présence du cycle benzénique.
1️⃣ 1ère partie : Influence du pH⚓
Complément : 📜 Document n°1 : Protocole expérimental
Dans un bécher de \(100\ \mathrm{mL}\), verser un volume \(V_1 = 30 \ \mathrm{mL}\) d'une solution d'acide chlorhydrique à la concentration \(c_1 = 1,0\cdot 10^{-2}\ \mathrm{mol\cdot L^{-1}}\).
À l'aide d'un pH-mètre préalablement étalonné, vérifier que le pH de la solution d'acide chlorhydrique est bien égal à 2.
Ajouter une masse \(m = 1,0\ \mathrm{g}\) d'acide benzoïque. Agiter la solution obtenue et mesurer le pH d e la solution.
Sous agitation, ajouter au goutte à goutte une solution d'hydroxyde de sodium \(\left( \ce{Na+} ; \ce{HO-}\right)\) à la concentration \(c_2= 1,0 \ \mathrm{mol\cdot L^{-1}}\), jusqu'à environ \(pH = 12\).
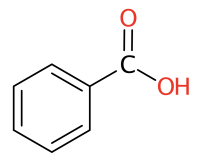
Complément : 📜 Document n°2 : Équation de réaction entre les ions hydroxyde HO- et l'acide benzoïque
Question⚓
Q3. À l'aide du site du l'INRS, rechercher les pictogrammes de sécurité et les mentions de dangers associés aux différentes substances utilisées. Indiquer alors les précautions à prendre.
Question⚓
Q4. Réaliser le protocole du document 1 et noter vos observations.
Question⚓
Q6. À l'aide de la structure de l'acide benzoïque et de l'ion benzoate, justifier la différence de solubilité observée lors de l'ajout d'hydroxyde de sodium à l'acide benzoïque.
2️⃣ 2ème partie : Influence de la température⚓
Question⚓
Q7. Dans deux béchers de \(100\ \mathrm{mL}\), verser \(50\ \mathrm{mL}\) d'eau distillée e t y ajouter une masse \(m = 1,0 \ \mathrm{g}\) d'acide benzoïque. Agiter le mélange. Observe-t-on la dissolution totale de l'acide benzoïque ?
Question⚓
Q9. Placer le second bécher dans un bain eau-glace en maintenant l'agitation jusqu'à atteindre une température d'environ \(0 \ \mathrm{^\circ C}\). Noter vos observations.
Question⚓
Q10. Indiquer l'influence de la température sur la solubilité de l'acide benzoïque dans l'eau.