💪🏻 Exercice 1️⃣ : Quantité de matière⚓
La vanilline est l'arôme naturel le plus important et le plus caractéristique de la vanille.
Une gousse de \(3\ \mathrm{g}\) peut contenir jusqu'à \(60\ \mathrm{mg}\) de vanilline.
Donnée : \(M_\textsf{vanilline} = 152 \ \mathrm{g\cdot mol^{-1}}\)
💪🏻 Exercice 2️⃣ : Masse molaire moléculaire⚓
Question⚓
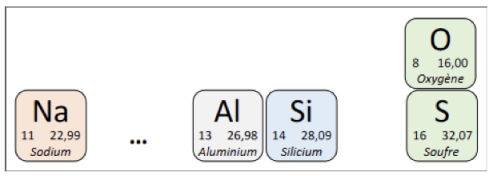
Q2. Calculer les masses molaires moléculaires des espèces chimiques suivantes :
dioxygène \(\ce{O2}\)
ammoniac \(\ce{NH3}\)
éthanol \(\ce{C2H6O}\)
acide lactique \(\ce{C3H6O3}\)
dichlorométhane \(\ce{CH2C\ell_2}\)
alanine \(\ce{C3H7NO2}\)
Solution⚓
Q2.
dioxygène \(\ce{O2}\) : \(M_{\ce{O2}}=32,0\ \mathrm{g\cdot mol^{-1}}\)
ammoniac \(\ce{NH3}\) : \(M_{\ce{NH3}}=17,0\ \mathrm{g\cdot mol^{-1}}\)
éthanol \(\ce{C2H6O}\) : \(M_{\ce{C2H6O}}=46,0\ \mathrm{g\cdot mol^{-1}}\)
acide lactique \(\ce{C3H6O3}\) : \(M_{\ce{C3H6O3}}=90,0\ \mathrm{g\cdot mol^{-1}}\)
dichlorométhane \(\ce{CH2C\ell_2}\) : \(M_{\ce{CH2C\ell_2}}=85,0\ \mathrm{g\cdot mol^{-1}}\)
:alanine \(\ce{C3H7NO2}\) : \(M_{\ce{O2}}=89,0\ \mathrm{g\cdot mol^{-1}}\)
💪🏻 Exercice 3️⃣ : Concentration en masse⚓
💪🏻 Exercice 4️⃣ : Concentration en quantité de matière⚓
Complément : 🗃️ Données
Masses molaires atomiques en \(\mathrm{g \cdot L^{-1}}\) : \(M(H) = 1,0\) ; \(M(C) = 12,0\) ; \(M(N) = 14,0\) ; \(M(O) = 16,0\).
Question⚓
L'aspartame est un édulcorant artificiel au fort pouvoir sucrant, synthétisé pour la première fois en 1965. On le retrouve notamment dans des sodas allégés en sucre, dits « light ». Sa formule semi-développée est la suivante :
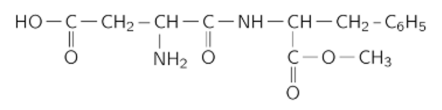
Pour ne pas dépasser la dose journalière admissible (DJA) d'aspartame (\(40\ \mathrm{mg}\) par \(\mathrm{kg}\) de masse corporelle et par jour), une personne de \(60\ \mathrm{mg}\) ne doit pas consommer plus de 280 sucrettes ou 20 canettes de boisson « light » par jour.
Q6. Déterminer la concentration en \(\mathrm{mol \cdot L^{-1}}\) en aspartame d'une canette de \(33\ \mathrm{cL}\) de boisson « light ».
💪🏻 Exercice 5️⃣ : Concentration en quantité de matière (encore)⚓
💪🏻 Exercice 6️⃣ : Dilution⚓
Au laboratoire, une technicienne doit préparer \(500,0 \ \mathrm{mL}\) d'une solution de peroxyde d'hydrogène \(\ce{H2O2}\) de concentration molaire \(C' = 5,0 \cdot 10^{-3}\ \mathrm{mol\cdot L^{-1}}\) Elle dispose d'une solution de concentration molaire \(C = 0,50\ \mathrm{mol\cdot L^{-1}}\)
💪🏻 Exercice 7️⃣ : Dissolution & Dilution⚓
Lors d'un TP un élève doit préparer, à partir d'un solide de formule brute \(\ce{C37H34N2Na2O9S3}\), un volume \(V = 250,0 \ \mathrm{mL}\) d'une solution de bleu brillant (colorant alimentaire E133) de concentration molaire en soluté \(c = 1,00 \cdot 10^{-2}\ \mathrm{mol\cdot L^{-1}}\).
💪🏻 Exercice 8️⃣ : Dosage du diiode par étalonnage⚓
Le Lugol est un antiseptique. Il contient du diiode \(\ce{l2}\). L'objectif est de déterminer la masse de \(\ce{l2}\), dans \(100\ \mathrm{mL}\) de solution de Lugol.
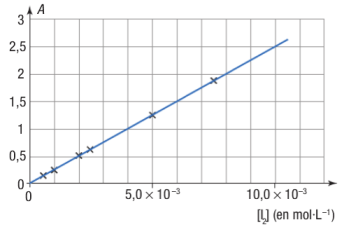
On mesure l'absorbance \(A\) de six solutions aqueuses de diiode de concentrations molaires en soluté différentes.
Les résultats de l'expérience permettent de tracer le graphique ci-contre →
La solution de Lugol a été diluée 10 fois. On mesure l'absorbance de la solution diluée : \(A = 1,00\).
💪🏻 Exercice 9️⃣ : Dosage par étalonnage d'une bouillie bordelaise⚓
La bouillie bordelaise est une solution aqueuse utilisée pour éliminer les champignons parasites sur les végétaux. Cette solution est bleue à cause de la présence d'ions cuivre (II) en solution, \(\ce{Cu2+}\), de concentration en masse voisine de \(200\ \mathrm{g\cdot L^{-1}}\)
On souhaite vérifier la concentration en ions cuivre (II) d'une bouillie bordelaise.
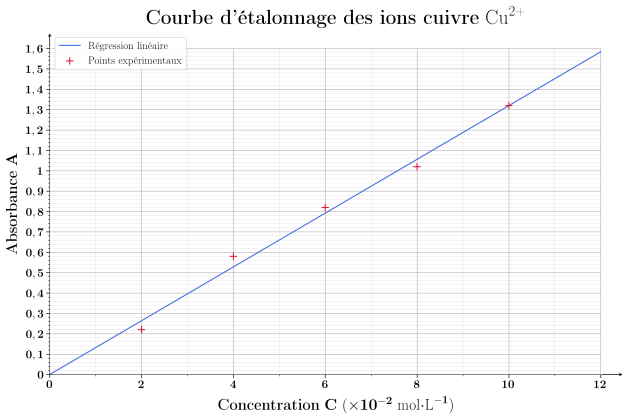
On utilise pour cela une solution mère d'ions cuivre (II) de concentration \(C_0 = 1,00 \cdot 10^{-1}\ \mathrm{mol\cdot L^{-1}}\) pour réaliser la courbe d'étalonnage colorimétrique.
Enfin, on dilue cent fois la bouillie bordelaise et on mesure son absorbance : on trouve \(A_0 = 0,40\).
Complément : Données :
Masse molaire de l'ion cuivre (II) : \(M_{\ce{Cu2+}}=63,5\ \mathrm{g\cdot mol^{-1}}\)
Complément : Graphiques
Question⚓
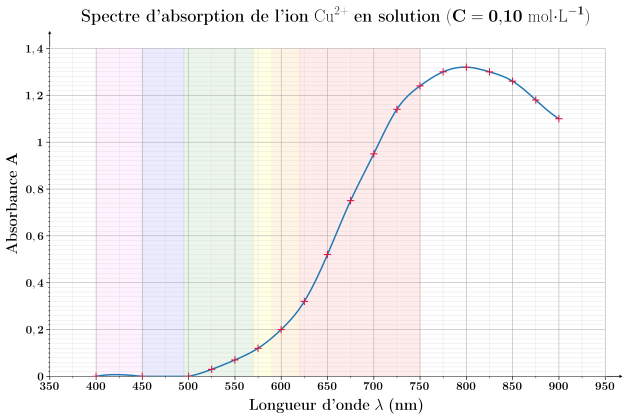
Q22. Déterminer sur le graphique d'étalonnage (Doc. 1), l'absorbance d'une solution de \(0,10\ \mathrm{mol\cdot L^{-1}}\). Vérifier sur le spectre d'absorption (Doc. 2) que la longueur d'onde choisie pour réaliser les mesures était bien \(\lambda = 800\ \mathrm{nm}\). Pourquoi avoir choisi cette longueur d'onde ?
💪🏻 Exercice 🔟 : Solubilité⚓
On donne le tableau suivant contenant les données suivantes :
Composé ;
Solubilité molaire à \(20\ \mathrm{^\circ C}\) en \(\mathrm{mol\cdot L^{-1}}\) ;
Solubilité massique à \(20\ \mathrm{^\circ C}\) en \(\mathrm{g\cdot L^{-1}}\) ;
Masse nécessaire de composé en \(g\) pour préparer \(50,0\ \mathrm{mL}\) d'une solution saturée à \(20\ \mathrm{^\circ C}\).
Composé | Solubilité molaire \(\left( \mathrm{mol \cdot L^{-1}} \right)\) | Solubilité en masse \(\left( \mathrm{g \cdot L^{-1}} \right)\) | Masse à peser (\(mg\)) pour préparer \(V = 50,0\ \mathrm{mL}\) d'une solution saturée |
|---|---|---|---|
\(\ce{Pb(SO4)}\) | \(1,4\cdot 10^{-4}\) | ||
\(\ce{C7H6O2}\) | 2,9 | ||
\(\ce{Cd(OH)2}\) | 13,0 |
Complément : Données
\(M(\ce{H}) = 1\ \mathrm{g\cdot mol^{-1}}\); \(M(\ce{C}) = 12\ \mathrm{g\cdot mol^{-1}}\); \(M(\ce{O}) = 16\ \mathrm{g\cdot mol^{-1}}\); \(M(\ce{S}) = 32\ \mathrm{g\cdot mol^{-1}}\) ; \(M(\ce{Cd}) = 112\ \mathrm{g\cdot mol^{-1}}\); \(M(Pb) = 207\ \mathrm{g\cdot mol^{-1}}\).