🧪 La tension superficielle des liquides⚓
🧪 Expérience à réaliser - 1ère partie
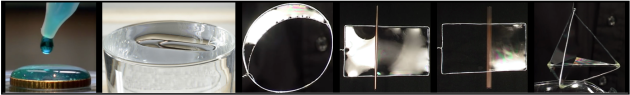
→ À l'aide d'une pipette, déposer délicatement des gouttes d'eau à la surface d'une pièce de monnaie.
→ Continuer jusqu'à ce que l'eau coule à côté de la pièce.
(On pourra poser la pièce sur un verre retourné, lui-même placé à l'intérieur d'une bassine ou sur une coupelle, afin de retenir l'eau).
Vidéo de l'expérience : 
🧪 Expérience à réaliser - 2ème partie
→ Très délicatement, déposer un trombone à la surface de l'eau dans un verre
🧪 Expérience à réaliser - 3ème partie
→ Tremper les différents supports métalliques à votre disposition dans un bac d'eau savonneuse. Crever la bulle d'un côté du fil ou de la petite barre.
Question⚓
Q5. (ANA) Qu'observez-vous avant de crever la bulle ?
Solution⚓
A1-Q5.
Une bulle de savon se forme à l'intérieur des supports. Le fil ou le barreau est en équilibre tant que la bulle n'est pas crevée. Mais dès qu'on crève la bulle sur un côté, le fil se tend du côté de la bulle restante. Pour la petite barre, elle se déplace du côté de la bulle restante.
Quant au tétraèdre, une bulle de savon ayant la forme d'une molécule de méthane \(\left(\ CH_4\ \right)\) se forme en son centre.
Question⚓
Q6. (APP/COM) Comment expliquer cela simplement ?
Solution⚓
A1-Q6.
La bulle de savon minimise sa surface, et tend le fil à cause de la tension superficielle. La bulle de savon peut tirer une petite barre et la mettre en mouvement, comme un petit ressort qui se contracte, encore grâce à la tension superficielle.
En ce qui concerne le tétraèdre, la forme de la bulle est très spéciale car elle minimise sa surface de contact avec l'air.
👨🎓 Quelques notions sur la tension superficielle⚓
📄 Documents⚓
Complément : [Document n°2] - Qu'est-ce que la tension superficielle ?
Les phénomènes observés précédemment sont dus à l'existence de forces existant à la surface libre du liquide.
Imaginons qu'on veuille créer à la surface libre d'un liquide une ouverture en forme de fente, de longueur L et de largeur \(\large \Delta x\) très petite : il faut pour cela exercer en plusieurs points de l'ouverture des forces \(\large {\vec{T_i}}\), qui doivent être des forces de traction. En effet, le liquide tend à s'opposer à cette opération en développant une force de norme \(\large F\) qui s'oppose aux forces \(\large {\vec{T_i}}\).
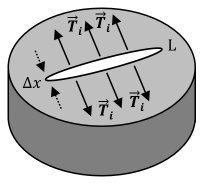
La norme \(\large F\) de la force \(\large \vec{F}\) est proportionnelle à la longueur \(\large L\) de la fente. On peut donc écrire :
\[\fbox{$ {\large { \text{ } F =\sigma \times L \text{ } }} $}\] Où \(\large \sigma\) est la tension superficielle, et se mesure en \(\mathrm{N.m^{-1}}\).
Remarque : on l'appelle aussi coefficient de tension superficielle.
La tension superficielle dépend du liquide, du milieu qui surmonte sa surface libre et de la température.
Remarque : Dans le cas d'un liquide présentant 2 faces en contact avec l'air, comme le cadre rempli d'une lame mince liquide avec la petite barre, on aura \(\large F=2\ \sigma \ L\).
Complément : [Document n°3] - Surface libre d'un liquide
Contrairement aux gaz, les liquides n'occupent pas tout le volume qui leur est offert lorsqu'ils sont contenus dans un récipient.
Les liquides possèdent ainsi une ou des surfaces libres.
Dans le cas des gaz, les molécules n'interagissent que par chocs, les forces de cohésion entre molécules sont donc inexistantes.
En revanche, pour les liquides, ce sont les forces de cohésion d'origine électromagnétique qui permettent aux molécules de rester voisines. Les molécules se situant à la surface libre ne possèdent pas autant de proches voisines que leurs homologues situés au sein du liquide.
La Fig.2 illustre la situation des molécules situées en surface (les flèches indiquent le sens des interactions subies par chaque molécule).
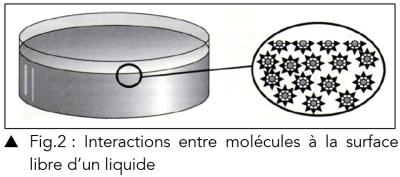
Les molécules situées en surface du liquide sont ainsi attirées vers ce dernier. L'énergie qu'il faut fournir pour accroître la surface libre du fluide de \(\large \Delta S\) est proportionnelle à une quantité appelée coefficient de tension superficielle notée \(\large \sigma\ \left(\mathrm{N.m^{-1}}\right)\) avec une énergie du type : \(\large \Delta E=\sigma\times \Delta S\). Ainsi, le liquide cherche à minimiser sa surface pour minimiser son énergie (c'est pour cela qu'en apesanteur, l'eau prend la forme d'une sphère dans une capsule spatiale).
❔ Questions⚓
Question⚓
Q8. (ANA) Que se passe-t-il pour les molécules en surface du liquide ? Quelle en est la conséquence visible ?
Solution⚓
A1-Q8.
Les molécules situées en surface du liquide sont ainsi attirées vers ce dernier. Ces molécules de surface se comportent donc comme une membrane tendue sur les autres molécules, comme pour les retenir, membrane qui comprime le liquide dans certains cas. D'où le terme de tension superficielle.
Question⚓
Q10. (ANA) Quelle différence y-a-t-il entre l'eau et la glycérine ? Comment cela se traduit-il ?
❔ Quel intérêt dans le domaine professionnel ?⚓
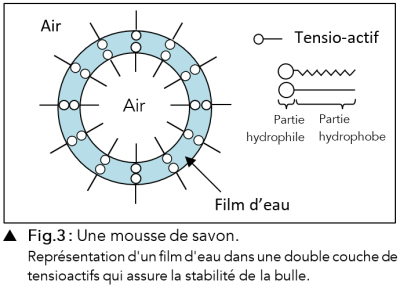
Complément : [Document n°4] - Les tensioactifs
Les agents tensioactifs abaissent la valeur de \(\large \sigma\) des liquides dans lesquels ils sont ajoutés et les rendent mouillants[*], moussants[*], détergents[*], émulsifiant[*]...
Si l'énergie de surface entre un solide et l'eau est importante, l'eau reste sous forme de gouttelettes : certains tissus laissent glisser l'eau. En ajoutant un agent tensioactif, l'énergie de surface diminue, la goutte s'étale et peut pénétrer dans le tissu.
Les émulsifiants sont des tensioactifs : pour garder l'huile d'une vinaigrette sous la forme de petites gouttelettes, ou émulsion, il faut diminuer la tension superficielle afin que le gain d'énergie de surface lorsque deux gouttes se réunissent soit faible.
Les tensioactifs permettent de stabiliser les bulles. Une bulle, formée dans un verre d'eau avec une paille, crève, lorsqu'elle atteint la surface. En ajoutant du sirop dans l'eau, la bulle reste à la surface. L'augmentation de surface due à la présence de la bulle ne provoque pas une grande augmentation d'énergie car \(\large \sigma\) est faible. C'est pourquoi les lessives, qui contiennent des agents tensioactifs pour favoriser la pénétration de l'eau dans les tissus, moussent facilement.
Question⚓
Q11. (ANA) Quel est l'intérêt des tensio-actifs dans le cas de la lessive ? Dans le cas de la vinaigrette ? Comment ?
Solution⚓
A1-Q11.
L'intérêt des tensio-actifs est de faire en sorte que la lessive mousse davantage, lui permettant de mieux pénétrer dans les fibres des tissus, ce qui nettoie mieux.
[Faire schémas d'une tâche avec le tensioactif]
Dans le cas de la vinaigrette, c'est pour garder l'huile sous forme de gouttelette.
Dans les deux cas, c'est en abaissant la valeur du coefficient de tension superficielle qu'on favorise la formation de bulles d'air pour la lessive ou d'huile dans la vinaigrette.
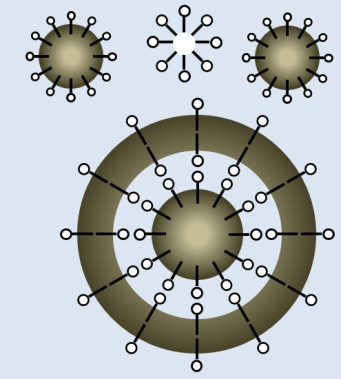
Question⚓
Q12. (ANA) Comment peut-on qualifier la partie de la molécule de tensio-actif qui reste dans l'eau pour la mousse de savon ? Et pour la partie qui reste dans l'air ?
Complément : [Document n°5] - Et dans les processus industriels ?
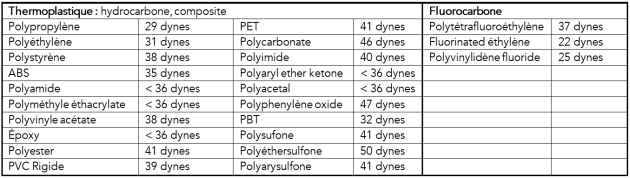
La tension superficielle est très importante notamment dans les processus industriels. Plus elle est élevée, plus l'adhésion d'une substance (colle, encre) appliquée sur le matériau sera bonne.
Une autre unité de mesure de la tension superficielle
On a vu précédemment que l'unité de mesure de la tension superficielle était le newton par mètre \(\left( \mathrm{\ N.m^{-1}\ }\right)\) qui est équivalent aux joules par mètre carré \(\left(\mathrm{\ J.m^{-2}\ }\right)\) qui est l'unité d'énergie de surface (ou \(\mathrm{{dyne}/{cm}}\) ).
La tension superficielle est donc la force qu'il faut appliquer à un liquide pour provoquer l'extension de sa surface. On peut définir l'énergie d'interface comme un surplus d'énergie chimique lorsque les molécules de surface se trouvent à l'intérieur du liquide.
Peut-on modifier le coefficient de tension superficielle ?
Une électrode, reliée à un générateur à haute fréquence et haute tension alternative, émet une décharge électrique sous forme d'effluve. Ce qui le modifie physiquement et chimiquement le matériau à traiter (adhérence des encres, colles...). En laboratoire on utilise un appareil à main, pratique pour les petites séries, et facilement installable (sur une prise standard). Industriellement il faut utiliser une station industrielle sur mesure, qui vont de quelques centimètres à plusieurs mètres, avec différents types de cylindres diélectriques et d'électrodes.
Question⚓
Q13. (ANA) Quelle peut être l'intérêt de connaitre/mesurer le coefficient de tension superficielle d'un matériau ?
Solution⚓
A1-Q13.
L'intérêt de connaître le coefficient de tension superficielle d'un matériau est de savoir si on peut y déposer une substance dessus pour qu'elle y adhère bien, comme par exemple l'encre, la colle... donc savoir s'il est imprimable ou collable (ou l'inverse).
Cela peut aussi servir à connaître la propreté d'un matériau.