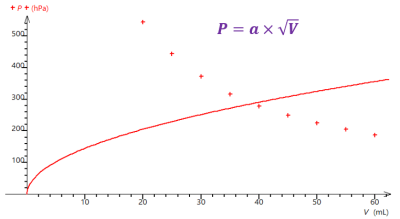
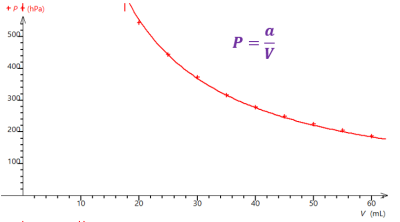
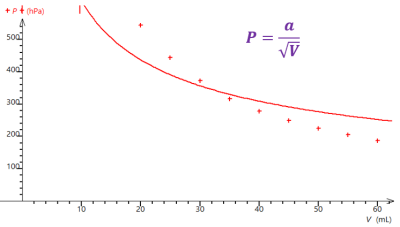
Un gaz est modélisé à l’échelle microscopique par un mouvement désordonné de particules.
Pourtant un gaz peut être caractérisé par des grandeurs macroscopiques :
La pression \(P\) ;
La température \(T\) ;
La quantité de matière \(n\).
🤔 Comment décrire un gaz parfait ?⚓
Définition : 📌 Le modèle du gaz parfait - [Document n°1]
Le gaz parfait est un modèle thermodynamique décrivant le comportement des gaz réels à basse pression.
Ce modèle a été développé du milieu du XVIIème siècle au milieu du XVIIIème siècle et formalisé au XIXème siècle. Il est fondé sur l'observation expérimentale selon laquelle tous les gaz tendent vers ce comportement à pression suffisamment basse, quelle que soit la nature chimique du gaz, ce qu'exprime la loi d'Avogadro, énoncée en 1811 : la relation entre la pression, le volume et la température est, dans ces conditions, indépendante de la nature du gaz.
Cette propriété s'explique par le fait que lorsque la pression est faible, les molécules de gaz sont suffisamment éloignées les unes des autres pour que l'on puisse négliger les interactions électrostatiques qui dépendent, elles, de la nature du gaz (molécules plus ou moins polaires). De nombreux gaz réels vérifient avec une excellente approximation le modèle du gaz parfait dans les conditions normales.
C'est le cas des gaz principaux de l'air, le diazote et le dioxygène.
Source : Wikipédia & https://fr.khanacademy.org
Question⚓
Q1. Décrire simplement ce qu’est un gaz parfait.
Solution⚓
Q1.
On appelle gaz parfait un ensemble de molécules sans interaction entre elles en dehors des chocs élastiques. Les molécules ne s’attirent ou ne se repoussent pas, elles ne font que se cogner les unes aux autres.
Les gaz parfaits ne constituent en fait qu’un modèle qui constitue bien souvent une approximation acceptable.
Exemple : 📑 Situations de la vie courante - [Document n°2]
Si on place un ballon partiellement dégonflé au soleil, on remarque qu’il reprend son volume initial et qu’il est plus dur.
La pression d’un gaz augmente avec la température.
La pression d’un gaz augmente aussi avec la quantité de matière du gaz.
Gonfler un ballon consiste à introduire de l’air dans le ballon. Le volume d’un gaz augmente aussi avec la quantité de matière du gaz qu’il contient.
Question⚓
Q2. Proposer une explication microscopique à chaque situation du document n°2.
Solution⚓
Q2.
Quand le ballon chauffe au soleil, l’énergie cinétique moyenne des molécules d’air augmente.
Elles bougent plus vite → elles frappent plus souvent et plus fortement la paroi du ballon.
La pression interne augmente → le ballon se regonfle (son volume augmente légèrement) et sa paroi devient plus tendue (sensation de dureté).
Les molécules d'air sont plus agitées car la température augmente, et prennent plus de place : le volume augmente. La pression augmente.
La température correspond à l’énergie cinétique moyenne des particules.
Plus \(T\) est élevée → plus les particules se déplacent vite.
Elles heurtent les parois plus souvent et avec plus de force → la pression \(P\) augmente (si le volume reste fixe).
Ajouter du gaz signifie introduire plus de particules.
À température et volume constants, il y a plus de particules qui viennent frapper les parois.
→ Le nombre total de chocs par unité de temps augmente → la pression P augmente.
Quand on souffle dans le ballon, on ajoute des particules d’air.
Comme le ballon peut se dilater, son volume augmente pour que la pression interne s’équilibre avec la pression extérieure.
Plus il y a de molécules → plus elles occupent d’espace → le ballon grossit.
📈 Variation de la pression en fonction du volume⚓
Lire les documents suivants puis répondre aux questions.
📄 Documents⚓
Complément : 📄 Pourquoi un paquet de chips gonfle-t-il lorsque l’altitude augmente ? - [Document n°3]

Les randonneurs et les alpinistes constatent que le volume des paquets de chips a tendance à augmenter au fur et à mesure qu’ils progressent en montagne. D’autre part, il est même délicat d’ouvrir un pot de yaourt car celui-ci devient « bedonnant » en altitude.
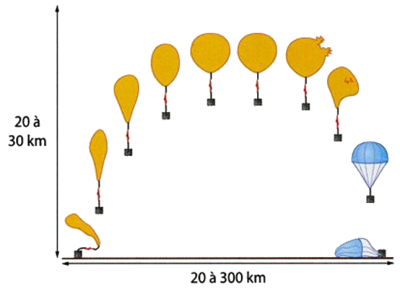
Complément : 📄 Les ballons sondes - [Document n°4]
Les ballons sondes sont utilisés en météorologie. Il s'agit d'un ballon libre non habité, utilisé pour faire des mesures de pression dans l'atmosphère grâce à des capteurs mis à bord dans une nacelle. Ils sont équipés d'un système de localisation GPS pour les suivre et donc déterminer entre autres la direction des vents.
Complément : 📄 Plongée sous-marine - [Document n°5]

Dans une bouteille de plongée, l’air est comprimé, c’est-à-dire qu’il est stocké sous grande pression. Le détendeur permet au plongeur de respirer de l’air à la même pression que celle de l’eau qui l’entoure. Cette pression de l’eau, qui augmente avec la profondeur, a une influence sur le volume des bulles d’air que le plongeur expulse en respirant.
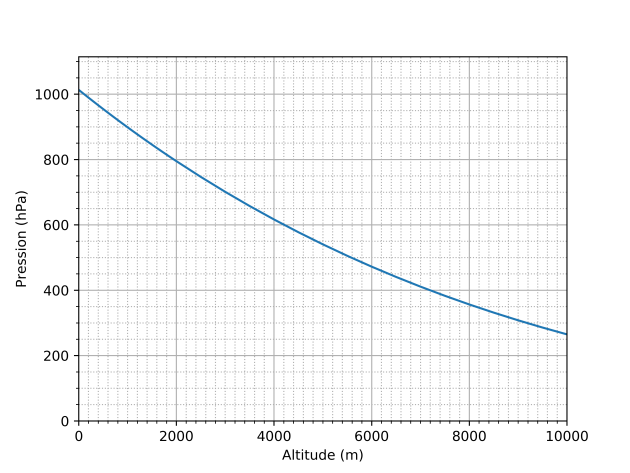
Complément : 📄 Variation de la pression en fonction de l’altitude - [Document n°6]
La pression (indiquée ici en hectopascals) est modifiée quand on s'élève en altitude. On suppose ici qu'il fait \(15\ \mathrm{^\circ C}\) au niveau de la mer, et que la pression y est de \(1\ 013\ \mathrm{hPa}\) (valeur de la pression atmosphérique normale). Quand le temps change, la courbe change légèrement de forme.
❓Questions⚓
🕹️ Simulation⚓
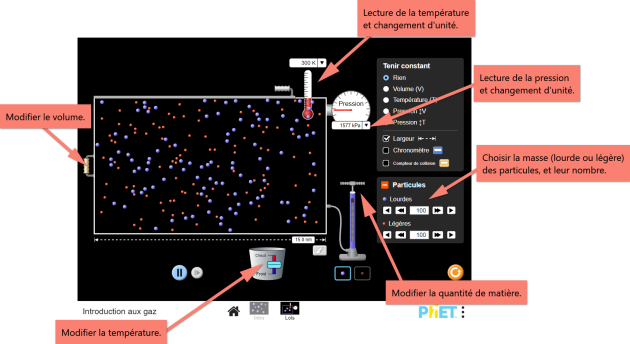
Complément : 🕹️ Simulation - [Document n°7]
Voici une simulation en ligne :
https://phet.colorado.edu/sims/html/gas-properties/latest/gas-properties_fr.html 
Les entités sont modélisées par des sphères.
On peut choisir léger ou lourd.
→ Familiarisez-vous avec l'animation.
🧪 Protocole expérimental
Dans la zone « Particules », ajouter 200 particules lourdes à la température \(T=300\ \mathrm{K}\) ;
Dans l'option des paramètres constants, choisir la température ;
Déplacez le curseur du récipient aussi loin que possible vers la gauche ;
Sélectionnez la règle (« Largeur ») dans l'option des outils de mesure ;
Afficher la pression en \(\mathrm{kPa}\) ;
Mesurer la longueur du récipient (attendre que la pression se stabilise) et estimer la pression moyenne ;
Effectuez le processus ci-dessus jusqu'à ce que vous ayez une dizaines de mesures différentes et écrivez les données dans un tableau de mesure. (voir tableau ci-dessous).
Pour la suite, on admettra que les deux autres côtés de l’enceinte font \(10\ \mathrm{nm}\). Rappel \(1 \ \mathrm{nm} = 10^{-9} \ \mathrm{m}\).
Alors, à l'aide d'un tableur-grapheur comme Regressi (ou Excel, ou LibreOffice Calc si Regressi n'est pas disponible), représentez graphiquement la pression en fonction du volume \(p=f(V)\).
Compléter ensuite les deux dernières lignes du tableau en s'aidant du tableur pour faire les calculs à votre place en une seule fois.
(Aide : Il faudra créer une grandeur calculée avec comme formule ce que vous voulez calculer.)
Question⚓
Q6. Compléter le tableau suivant à l’aide de la simulation.
📏 Tableau de mesures
Largeur en \(\mathrm{nm}\) | 15 | 14 | 13 | 12 | 11 | 10 | 9 | 8 | 7 | 6 | 5 |
Volume \(\mathrm{V\ \left(en \ m^3 \right)}\) | |||||||||||
\(\mathrm{p\ \left(en\ Pa \right)}\) |
Question⚓
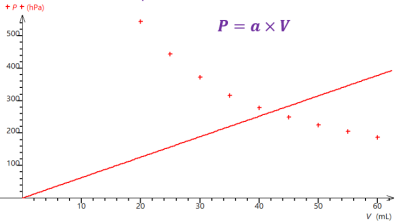
Q10. À l'aide d'un tableau/grapheur, représenter graphiquement l’évolution de la pression \(p\) en fonction du volume \(V\) : \(p=f\left( V \right)\).
Reproduire sommairement ci-contre votre graphique
Conclusion
Définition : 📌 La loi des gaz parfaits
💭 Cette loi sur le comportement des gaz est la loi de Boyle-Mariotte établie au XVIIème siècle par l’irlandais Robert Boyle et validée par le physicien français Edme Mariotte en 1676.
Question⚓
Q13. Les résultats obtenus lors de cette expérimentation sont-ils cohérents avec les autres documents proposés. Argumenter votre réponse. Préciser ce qu’il advient du ballon-sonde à une certaine altitude.
Solution⚓
Q13.
Doc.5 : Le volume du paquet de chips augmente car en altitude la pression diminue.
Doc.6 : Le volume du ballon-sonde augmente lorsqu’il monte dans les hautes couches de l’atmosphère car la pression diminue. Il finit même par éclater à une certaine altitude et la nacelle redescend en parachute.
Question⚓
Q14. Préciser ce qu’il advient du ballon-sonde du document n°4 à une certaine altitude.
Solution⚓
Q14.
Comme la pression extérieure baisse avec l'augmentation d'altitude, le volume du ballon augmente : le gaz à l’intérieur du ballon se dilate.
Le ballon grossit fortement, puis arrive une altitude où la membrane du ballon atteint sa limite d’élasticité : le ballon éclate, et la nacelle retombe au sol.
🏋️ Exercice⚓
Question⚓
Un ballon gonflé à l’hélium contient une quantité de matière \(n = 0,40\ \mathrm{mol}\) d’hélium. Il s’élève à une où la pression est \(p = 701 \ \mathrm{hPa}\), et une température \(T = 253 \ \mathrm{K}\).
Donnée : \(R = 8,31 \ \mathrm{Pa\cdot m^3 \cdot mol^{-1} \cdot K^{-1}}\).
Q15. Calculer le volume du ballon à cette altitude.
Question⚓
Un pneu de vélo de volume \(V = 2,5\ \mathrm{L}\) contient un gaz. La pression est \(p = 350 \ \mathrm{kPa}\), et la température est \(\theta = 20 \ \mathrm{^\circ C}\).
Donnée : \(R = 8,31 \ \mathrm{Pa\cdot m^3 \cdot mol^{-1} \cdot K^{-1}}\).
Q15. Calculer la quantité de matière de gaz n dans le pneu